日本における
オートファジー研究について

1
オートファジー研究の
ブレイクスルー
APGOの技術顧問テクニカルアドバイザーの吉森は、細胞生物学者です。細胞内の交通網が専門で、1996年からはその中でもオートファジーの研究を集中的に行っています。オートファジー研究分野のパイオニアである大隅良典先生が、この年に愛知県岡崎市にある国立の基礎生物学研究所教授になられ、吉森を助教授として呼ばれたことがきっかけでした。 オートファジーは、1950年代には存在が知られていましたがその後長く研究が進展せず、謎に包まれたまま残されていました。大隅先生は酵母を実験材料にこの未開拓の分野に挑戦され、画期的な成果をあげられました。大隅先生はまず酵母の細胞にもヒトなどと同じオートファジーがあることを見つけられ、続いて遺伝学的な研究がしやすい酵母の利点を活かしてオートファジーに必要な遺伝子群を発見されました1。 遺伝子は、タンパク質の設計図です。タンパク質は栄養にもなりますが、細胞の中の社会においては我々の社会の人間にあたる役割を果たしています。つまり、細胞の中には数万種類のタンパク質がいて各々違う職能を持って働いているのです。 大隅先生はオートファジーに働くタンパク質14種類の遺伝子を見つけられました。 遺伝子が見つかるとその設計図から作られるタンパク質の働きを調べることができます。この発見がブレイクスルーとなり、その後オートファジー研究が世界中で活発になりました。大隅先生は、この功績により2016年にノーベル生理学医学賞を受賞されました。
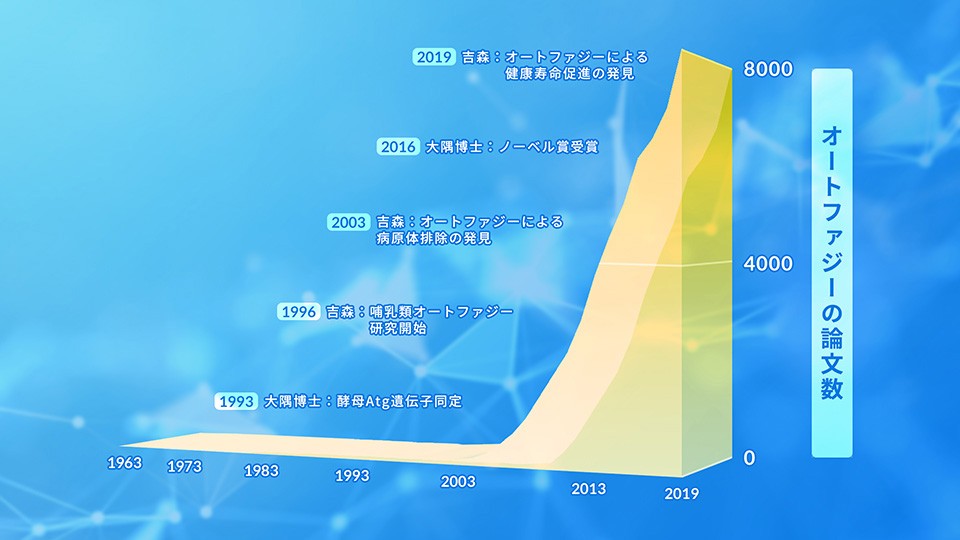

オートファジー分野の論文数の推移
世界で出される論文の数でその分野が活発かどうかが判ります。大隅先生の発見をきっかけに今もオートファジー分野は急成長を続けています。
2 酵母から哺乳類へ
大隅先生は酵母がご専門ですが、将来オートファジーの研究はヒトを含む哺乳類で発展するだろうと予見されました。そこで、哺乳類を専門とする吉森を助教授に選ばれました。吉森は、大隅先生の酵母の成果を手がかりに哺乳類オートファジーの仕組みの解明を開始しました。 そして吉森が哺乳類のオートファゴソームに結合するタンパク質を世界で初めて見つけた2結果、哺乳類のオートファジー研究が発展します。そのタンパク質LC3がオートファゴソームの目印に使えたからです。LC3は今でも世界中で使われており、吉森のLC3発見の論文はこの分野で最も沢山引用されています。 哺乳類オートファジーの研究が進むと、次の章で述べるようにオートファジーが病気を防ぎ健康を維持するために大事であることが分かって来ました。その結果、現在世界で年間7,000報以上出されるオートファジー関連の論文の多くは哺乳類を扱っています。大隅先生の予見は当たったのです。そして病気の治療予防や健康増進に役立つ可能性が出てきたことが、先生のノーベル賞受賞を後押ししたことは間違いがありません。 吉森は他にもオートファジーのメカニズムに関する重要な発見を数多く行っていま す。後で述べるオートファジーのブレーキ役のタンパク質Rubiconの発見3もそうで す。また、上述の皮膚の色を決めるメカニズムも企業との共同研究で明らかにしました。
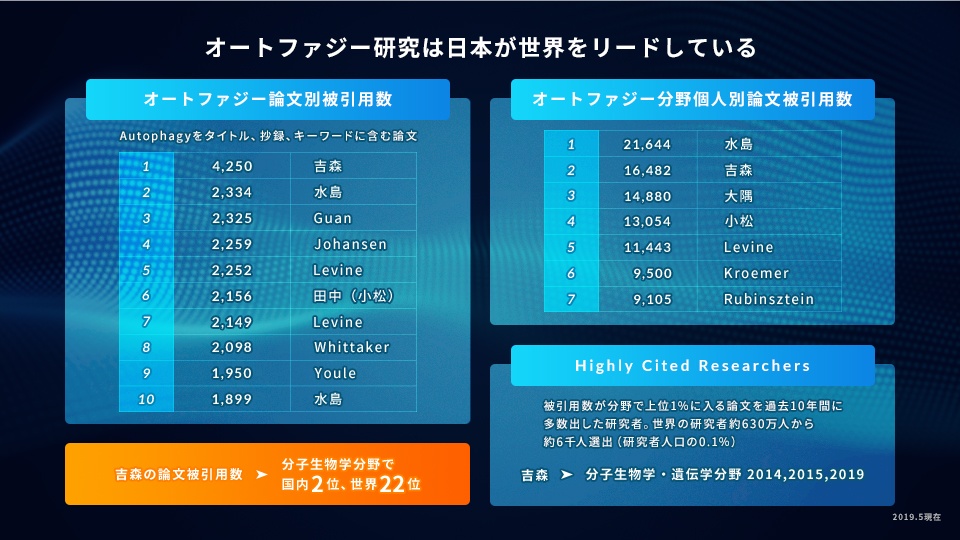

オートファジー研究は日本が世界をリードしている
他の人の論文に多く引用される論文は優れた論文と考えられます。日本人のオートファジーの論文は世界で沢山引用されます。日本がこの分野の頂点に立っていることが判ります。吉森のLC3論文が分野で一位で、また吉森の論文の総被引用数は、オートファジーに限らない分子生物学という広い範囲で国内2位、世界22位をマークしています。
3
オートファジーの
重要性が
分かってきた
吉森は、オートファジーと病気の関係についても数多くの成果をあげてきました。既に述べたオートファジーによる病原体の排除も吉森の発見です4。細胞内に侵入した病原体を排除することはできないとそれまでは言われていたので、この発見は画期的でした。しかも、免疫に働く細胞ではなくてもどんな細胞でも起こる現象なので、ヒトにとって非常に重要な免疫システムのひとつとみなされています。この発見のももうひとつ大事なポイントは、無作為に細胞の成分を分解しているだけと考えられていたオートファジーに第2の役割、すなわち有害物を選択的に取り込んで分解するという機能があることが判明したことです。この発見以降、神経変性疾患の原因となるタンパク質の塊や、心不全や発がんなど様々な病気の原因となる壊れたミトコンドリアなど様々な有害物がオートファゴソームに認識され隔離されることが次々と見つかりました。また、オートファジーは病原体を直接排除するだけではなく、免疫システムを構成する免疫細胞を作ることや免疫システム内の情報の伝達にも関わっています。従って免疫力を高め維持するためにはオートファジーが必要です。
4
オートファジーの
ブレーキ
Rubiconの発見
上述のように高脂肪食(脂っこい食事)を食べたり、歳を取るとオートファジーが低下し、それが病気をおこしたり悪化させたりします。このようなとき、どうしてオートファジーが低下するのでしょうか? 吉森はその原因がRubiconというタンパク質が増えるためだと言うことを突き止めました。Rubiconは吉森が発見したタンパク質で、大隅先生が発見したAtgというタンパク質群が全てオートファジーに必要なものであるのと対照的に、オートファジーを低下させる働きがあります。 特定のタンパク質を持たない動物を作る実験技術を用いて、吉森が肝臓のRubiconが無いマウスを作ったところ、高脂肪食を与えてもオートファジーが低下せず脂肪肝にもなりませんでした5。この結果は、Rubiconの増加がオートファジーの低下による脂肪肝の主要因であることを示しています。 また線虫やショウジョウバエなどの実験動物でRubiconを無くすと、寿命が1.2倍延び、かつ加齢による活動の低下や神経変性疾患が改善されました6。Rubiconの無いマウスも、パーキンソン病や腎臓の線維化などの加齢に伴って増える病気になりにくくなることが判りました。この研究成果はマスメディアからも注目され、主要新聞全てとNHKニュースで取り上げられました。
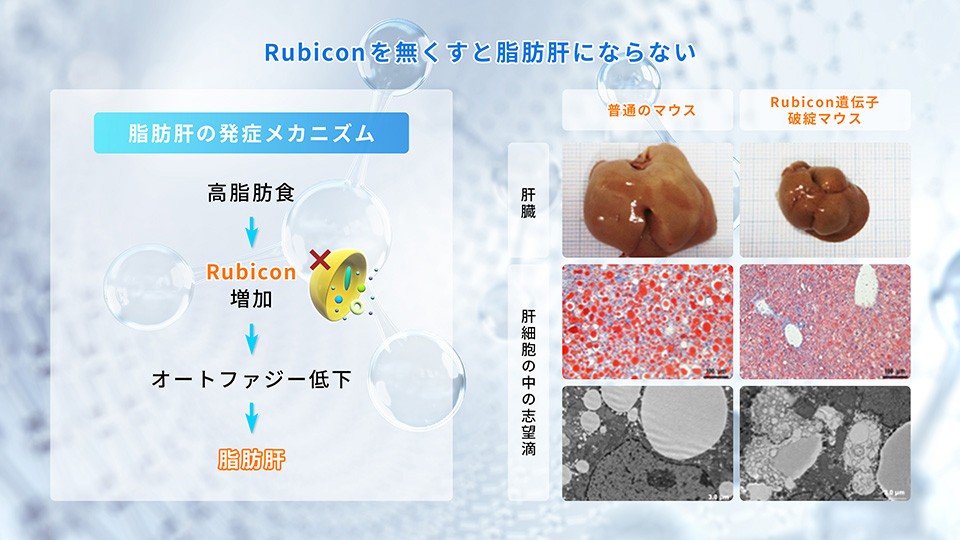

左上:Rubiconの増加で脂肪肝に
Rubiconの遺伝子を破壊するとタンパク質であるRubiconが作られなくなります。ここでは肝臓のRubicon遺伝子を破壊しています。
右下:Rubiconは老化でも増加する
歳を取るとRubiconが増え、オートファジーが低下します。Rubicon遺伝子破壊(KO)動物は、寿命が延び、加齢性の病気になりにくくなります。
参考文献
1. FEBS Lett. 1993 333:169-74.
2. EMBO J. 2000 19:5720-8.
3. Nat Cell Biol. 2009 11:385-96.
4. Science 2004 306:1037-40.
5. Hepatology. 2016 64:1994-2014
6. Nat Commun. 2019 10:847.

